Найден маленький рибозим-полимераза, способный реплицировать сам себя
Согласно теории РНК-мира, на ранних этапах абиогенеза важную роль играли рибозимы-полимеразы — молекулы РНК, способные размножать молекулы РНК, в том числе самих себя. До сих пор ученым удавалось получить (вывести путем искусственной эволюции или целенаправленно спроектировать) только крупные рибозимы-полимеразы длиной более 150 нуклеотидов, ни один из которых не мог реплицировать сам себя. Вероятность случайной самосборки таких больших молекул исчезающе мала, сами они недолговечны, а для их устойчивого размножения и дальнейшей эволюции необходима труднодостижимая скорость и точность репликации. Британские ученые сделали важный шаг к преодолению этих трудностей. Использовав новые методы отбора, они вывели из случайных молекул РНК маленький рибозим-полимеразу QT45 длиной всего в 45 нуклеотидов, способный к саморепликации. Исследование показало, что в пространстве последовательностей РНК мотивы с полимеразной активностью встречаются намного чаще, чем предполагалось. А главное, среди них есть совсем маленькие. Это делает более правдоподобной идею об их эволюционном возникновении посредством неферментативной репликации и даже позволяет допустить случайную самосборку готового рибозима-полимеразы.
1. Роль рибозимов-полимераз в мире РНК
Последние достижения в развитии теории мира РНК (см. ссылки в конце новости) позволяют считать, что начальные этапы зарождения жизни, вероятнее всего, были следующими:
1) Абиогенный синтез нуклеотидов в геотермальных системах из смеси простейших абиогенных углеводов и азотистых соединений.
2) Олигомеризация: синтез случайных коротких олигонуклеотидов на минеральных матрицах, с возможным участием аминокислот в качестве катализаторов и важной ролью циклов обводнения-высыхания в геотермальных системах.
3) Неферментативная репликация — возможно, путем матричного лигирования в слабощелочных условиях (см. Аминокислоты помогают нуклеотидам соединяться в короткие молекулы РНК, «Элементы», 16.07.2025). Старт дарвиновской эволюции.
4) Эволюция рибозимов, в том числе полимераз — молекул РНК, катализирующих размножение (репликацию) других молекул РНК и самих себя. Рибозимы-полимеразы, эволюционируя, повышают скорость и точность репликации, что подстегивает прогрессивную эволюцию живых систем.
5) Эволюция сложных РНК-организмов и программируемого синтеза белков.
Если бы этап 2 протекал очень бурно, а первые эффективные рибозимы из этапа 4 были совсем маленькими, то в принципе можно было бы даже пропустить этап 3. Иначе говоря, первые достаточно эффективные рибозимы-полимеразы могли бы собраться из нуклеотидов «случайно», без помощи наследственности и отбора.
В любом случае рибозимы-полимеразы должны были играть ключевую роль на определенном этапе абиогенеза. Поэтому их активно изучают. У современных живых организмов таких рибозимов нет. Их давно вытеснили гораздо более эффективные белковые полимеразы. Но в прошлом они были, а значит, их можно воссоздать.
Ученые ищут последовательности нуклеотидов с полимеразной активностью в бескрайнем пространстве последовательностей (см. Sequence space (evolution)), выбирая перспективных кандидатов из множества случайных молекул РНК. Затем пытаются улучшить рабочие качества этих кандидатов при помощи искусственной эволюции (внесение случайных мутаций — отбор наилучших — следующий раунд размножения с мутациями и т. д.), комбинируя эволюционный подход с элементами сознательного проектирования (см. Рибозимы могут размножать друг друга, «Элементы», 13.04.2011).
Год за годом мы наблюдаем в этой области впечатляющий прогресс. Например, недавно удалось повысить точность работы рибозима-полимеразы до уровня, достаточного для обеспечения настоящей прогрессивной эволюции другого рибозима, правда очень маленького — эндонуклеазы Hammerhead (см. Эволюция рибозимов, размножаемых рибозимами: еще один шаг к воссозданию РНК-жизни в пробирке, «Элементы», 27.03.2024).
2. Почему так важно найти маленький рибозим-полимеразу
Все достижения в изучении рибозимов-полимераз до сих пор были связаны с большими, громоздкими молекулами длиной более 150 нуклеотидов. Начинало даже закрадываться подозрение, что молекула РНК меньшего размера вообще не может иметь полимеразной активности. Это вело к пессимистичным (то есть низким) оценкам вероятности абиогенеза и частоты встречаемости жизни во Вселенной по нескольким причинам:
1) Вероятность случайной самосборки конкретной последовательности из 150 нуклеотидов исчезающе мала. Возможных последовательностей такой длины существует 4150 ≈ 1090. Это сопоставимо с числом элементарных частиц в наблюдаемой Вселенной. Дарвиновская эволюция на основе неферментативной репликации тоже вряд ли смогла бы вывести такого 150-нуклеотидного монстра, если до достижения этого размера он не помогал реплицировать РНК.
2) Чтобы 150-нуклеотидная молекула могла нормально воспроизводиться и эволюционировать, не деградируя и накапливая полезные мутации, требуется очень высокая точность репликации. Нужно, чтобы в среднем было не более двух-трех ошибок на копию рибозима. Рибозимы-полимеразы, способные синтезировать 150-нуклеотидную молекулу с такой точностью, пока не найдены.
3) Даже без учета требований к точности репликации, рибозимам-полимеразам трудно реплицировать длинные матрицы, особенно если в них используются все 4 нуклеотида в произвольном порядке. Поэтому ни один из известных рибозимов-полимераз до сих пор не мог реплицировать сам себя (хотя некоторые подошли к этому довольно близко окольными путями, ).
4) Молекулы РНК недолговечны, в том числе в условиях, считающихся «пребиотически правдоподобными». Длинные молекулы, как правило, деградируют быстрее коротких. Это повышает требования к скорости работы полимеразы. Ведь для устойчивого самовоспроизводства она должна успеть за свою недолгую жизнь создать хотя бы одну-две полноценные копии самой себя. Известные рибозимы-полимеразы неторопливы: для копирования одной длинной молекулы РНК им обычно требуются даже не часы, а дни, что сопоставимо с периодом полураспада самого рибозима.
В свете этих фактов понятно желание исследователей под руководством Филиппа Холлигера (Philipp Holliger), известного специалиста по абиогенезу, найти радикально более короткий рибозим-полимеразу. Если земная жизнь — не нечто абсолютно уникальное, что может случайно появиться лишь в одной из бесчисленных вселенных Мультиверса, в пространстве последовательностей РНК должны существовать более короткие и изящные полимеразы, чем те неулюжие 150–200-нуклеотидные молекулы, с которыми ученые возились до сих пор.
3. Как родился совсем крохотный рибозим QT45
Исследователи не стали пытаться укоротить какую-то из известных полимераз. Они решились на более смелый шаг и начали поиск «с нуля», то есть с набора случайных коротких последовательностей. Точнее, с трех наборов случайных РНК разной длины: по 20, 30 и 40 нуклеотидов. В каждом наборе было примерно по шесть триллионов (6 · 1012) уникальных последовательностей. Это соответствует полному покрытию всего пространства последовательностей только для самых коротких молекул длиной в 20 нуклеотидов. Для 30-нуклеотидных молекул было охвачено лишь несколько миллионных, для 40-нуклеотидных — несколько триллионных от общего числа возможных последовательностей.
Первичный отбор последовательностей, обладающих хотя бы намеком на полимеразную активность, производился следующим образом (рис. 2). К каждой случайной молекуле (потенциальному рибозиму) присоединяли через гибкий РНК-овый мостик молекулу «субстрата» (олигонуклеотид, активированный тремя фосфатами на 5’-конце). Добавляли праймер (другой олигонуклеотид с молекулой биотина на 5’-конце) и матрицу — молекулу РНК, комплементарную субстрату и праймеру. Если потенциальный рибозим успешно проводил лигирование, то есть пришивал субстрат (а заодно и самого себя) к праймеру, то этот рибозим потом отлавливали благодаря наличию биотина на 5’-конце праймера. Это классическая методика, основанная на том, что биотин прилипает к шарикам, покрытым биотин-связывающим белком стрептавидином.

Рис. 2. Конструкция, использовавшаяся для первичного отбора последовательностей с минимальной способностью сшивать (лигировать) олигонуклеотиды, комплементарные матрице. Рисунок из обсуждаемой статьи.
Перед отобранными таким способом последовательностями в последующих раундах отбора ставили всё более сложные задачи, постепенно приближая отбираемые рибозимы к конечной цели: способности реплицировать любые матрицы путем последовательного присоединения комплементарных тринуклеотидов (триплетов).
Исследователи использовали в качестве «субстратов» не отдельные нуклеотиды, а триплеты, потому что из множества предыдущих работ постепенно становится ясно, что это — перспективный путь. Вот некоторые соображения в пользу триплетов (или других коротких олигомеров, но не одиночных нуклеотидов) в качестве субстратов для репликации в РНК-мире:
1) Триплеты комплементарно присоединяются к матрице в разных местах, мешая матрице сворачиваться в шпильки. Это упрощает репликацию молекул РНК со сложной трехмерной структурой.
2) Тот же механизм помогает справляться с проблемой повторного спаривания матриц с синтезированными на них комплементарными репликами.
3) Разных триплетов не так много — всего 64. Гипотеза о том, что все они могли в достаточной концентрации присутствовать в «колыбели жизни», не выглядит невероятной (см. Аминокислоты помогают нуклеотидам соединяться в короткие молекулы РНК, «Элементы», 16.07.2025).
4) Если эволюция репликации РНК начиналась с неферментативного матричного лигирования олигонуклеотидов, то логично, что первые рибозимы — РНК-полимеразы — тоже продолжали работать с олигонуклеотидами. Им незачем было переключаться на одиночные нуклеотиды, с которыми у них сразу стало бы больше проблем.
5) Есть интереснейшая линия гипотетических построений, согласно которой в РНК-мире существовала трипликаза — рибозим, который реплицировал РНК путем последовательного присоединения триплетов. Возможно, трипликаза отрезала эти триплеты от специальных маленьких РНК — переносчиков триплетов и по совместительству предков тРНК. Этот механизм репликации впоследствии лег в основу механизма трансляции, а сама трипликаза стала малой субъединицей рибосомы (). Гипотеза трипликазы родилась из изучения рибосомы и попыток понять происхождение трансляции. Изначально она никак не была связана с тем, что специалисты по неферментативной репликации и рибозимам-полимеразам заметили, что с триплетами работать проще, чем с одиночными нуклеотидами.
За 11 раундов отбора исследователям удалось вывести три непохожих друг на друга коротких рибозима-полимеразы, худо-бедно справляющихся с репликацией разнообразных матриц. Все три происходили из набора 40-нуклеотидных последовательностей. 20- и 30-нулеотидные молекулы, по-видимому, всё-таки слишком коротки, чтобы проявлять полимеразную активность.
С этими тремя кандидатами стали работать дальше, внося случайные мутации, ставя всё более жесткие критерии отбора и добавляя капельку сознательного проектирования. После семи дополнительных раундов отбора (суммарно — 18 раундов) исследователи пришли к симпатичному 51-нуклеотидному рибозиму-полимеразе (рис. 3, B), который потом удалось сократить до 45-нуклеотидного почти без ущерба для функциональности. Итоговый рибозим получил название QT45 (QT — аббревиатура слов Quite Tiny — «cовсем крохотный»).

Рис. 3. Сравнение одного из лучших полученных ранее рибозимов-полимераз 5TU/t1.5 (димер из двух молекул РНК длиной 152 и 136 нуклеотидов) и нового 51-нуклеотидного рибозима QT51 (который потом сократили до 45-нуклеотидного QT45). Рисунок из дополнительных материалов к обсуждаемой статье
Успеху способствовали следующие удачные решения:
- Авторы не пытались «довести до ума» и сократить уже известные огромные рибозимы-полимеразы, а провели целенаправленный поиск коротких мотивов буквально с нуля, из хаоса, как в первый день Творения. Это позволило довольно тщательно прочесать пространство коротких нуклеотидных последовательностей.
- Использование условий, облегчающих работу рибозимов-полимераз: реакции проходили в слабощелочном эвтектическом льду (см. Eutectic system). В заполненных жидкостью микрополостях льда достигается высокая концентрация реагентов, а рибозимы на холоде более стабильны.
- Выбор в качестве субстратов не мононуклеотидов, а триплетов (см. выше).
- Удачная схема отбора с гибким соединительным мостиком и биотинилированным праймером (рис. 2). Это позволило превратить даже слабую каталитическую активность в надежно отлавливаемый сигнал.
4. Свойства рибозима QT45
QT45 — представитель совершенно нового класса рибозимов-полимераз, не похожий по своей структуре на изучавшиеся ранее. Он может реплицировать матрицы с практически любой последовательностью нуклеотидов, потому что его работа не связана с образованием каких-либо Уотсон-Криковских связей (см. Спаренные основания) с комплексом «матрица-праймер-субстрат».
Дополнительные эксперименты показали, что для правильного взаимодействия QT45 с этим комплексом важны 2’-OH группы (то есть гидроксильные группы, присоединенные ко второму атому углерода в рибозе, см. Структра РНК) некоторых нуклеотидов матрицы, праймера и субстрата, расположенных на расстоянии от 1 до 4 нуклеотидных позиций от места лигирования. Похожая картина характерна и для некоторых больших рибозимов-полимераз, изучавшихся ранее. По-видимому, это говорит о том, что разные классы рибозимов-полимераз имеют конвергентно сходные способы обхватывания комплекса «матрица-праймер-субстрат» и взаимодействия с ним. Также из этого следует, что эти рибозимы вряд ли подходят для репликации ДНК, ведь наличие 2’-OH групп — это как раз то, что отличает рибонуклеотиды от дезоксирибонуклеотидов.
QT45 не слишком привередлив в выборе субстратов. Он может использовать для синтеза комплементарной нити РНК не только триплеты, но и более длинные олигонуклеотиды, активированные тремя фосфатами на 5’-конце. Также он может, хоть и с меньшим успехом, использовать динуклеотиды и даже отдельные мононуклеотид-трифосфаты. Не возражает он и против смесей всех этих субстратов в разных пропорциях, а также триплетов, активированных не тремя фосфатами, а двумя фосфатами и аденозином (что считается чуть более «пребиотически правдоподобным» вариантом). Такая неразборчивость делает более весомым предположение, что рибозимы, подобные QT45, могли участвовать в ранних этапах эволюции РНК-мира в «пребиотическом бульоне», где было намешано много всякой абиогенной органики.
Исследователи тщательно изучили ландшафт приспособленности (см. Fitness landscape) QT45. Иными словами, они проверили, как влияют на его «приспособленность» (функциональность) различные мутации. Рибозимы-мутанты должны были реплицировать матрицу, последовательно присоединив к праймеру три триплета UGC. Успешность выполнения этой задачи считалась мерой приспособленности. Объем работы, проделанный исследователями, впечатляет: они проверили все возможные однонуклеотидные замены (3 · 45 = 135 вариантов) и делеции (45 вариантов), а также 98% двойных замен (которых всего возможно 3 · 45 · 3 · 44 = 17 820 вариантов).
Анализ показал, что рибозим QT45 находится на вершине четко выраженного «пика приспособленности». Иными словами, большинство мутаций сильно снижают его функциональность (рис. 4). Но всё-таки не все: например, двойные мутации в участках, образующих двойную спираль, часто оказываются невредными, если сохраняется Уотсон-Криковская связь (например, комплементарная пара A-U заменяется на G-C).

Рис. 4. Влияние одиночных мутаций (однонуклеотидных замен и делеций) на функциональность рибозима-полимеразы QT45. Темно-красный цвет соответствует резкому снижению функциональности, светло-желтый — ее сохранению. Рисунок из обсуждаемой статьи
5. Схлопывание вселенной невероятности (лирическое отступление)
Вероятность случайной самосборки какой-то конкретной 150-нуклеотидной последовательности сопоставима с единицей, деленной на число элементарных частиц во Вселенной, включая фотоны и нейтрино (1090). Попросту говоря, такое событие невероятно, если не привлекать концепцию Мультивселенной, а это нежелательный прием в научном рассуждении. Конечно, в пространстве 150-нуклеотидных последовательностей много разных РНК-полимераз, и это наверняка избавляет нас от десятка-другого порядков невероятности. Но даже 1070 — число довольно безнадежное. Это число нуклонов в крупной галактике. Всё равно похоже на полную невероятность.
Что меняется в этих не очень серьезных (игнорирующих возможность эволюции на основе неферментативной репликации) расчетах благодаря открытию 45-нуклеотидной полимеразы? На первый взгляд может показаться, что разница не принципиальная: подумаешь, размер полимеразы уменьшили втрое. Но это обманчивое впечатление, ведь мы имеем дело с комбинаторикой и степенной функцией. Число всех возможных 45-нуклеотидных последовательностей — 1027. Это не в три, а в 1063 раз меньше, чем число возможных 150-нуклеотидных последовательностей. Это сразу перебрасывает нас из Макрокосма в Микрокосм. 1027 — это уже не про число элементарных частиц во Вселенной, а, скорее, про число атомов в одном-единственном человеческом теле.
С учетом результатов анализа ландшафта приспособленности QT45, его толерантности к мутациям, а также того, что среди примерно 1013 случайных 40-нуклеотидных последовательностей (из 1024 возможных) нашелся даже не один, а целых три разных РНК-полимеразных мотива (два других остались пока неизученными), — с учетом всего этого авторы считают, что можно смело отбросить еще десяток порядков, и тогда вероятность того, что случайная последовательность длиной в 40 или более нуклеотидов будет проявлять заметную РНК-полимеразную активность, можно считать равной примерно 10−16.
Это уже сущие пустяки. 1016 случайных молекул РНК могли содержаться в одном ведре «пребиотического бульона» в какой-нибудь геотермальной системе, где шли процессы, подобные описанным в новости Аминокислоты помогают нуклеотидам соединяться в короткие молекулы РНК («Элементы», 16.07.2025).
«Вселенная невероятности» схлопнулась до размеров геотермальной лужи. Скромной лужи где-нибудь на холодном протоматерике. Почему на холодном? Потому что нам пригодится немного льда по берегам.
6. Первые подвиги QT45: репликация РНК с двуспиральными участками и размножение маленького рибозима
Серьезную трудность для рибозимов-полимераз представляют матрицы с двуспиральными участками. Если эти участки уже скручены в двойную спираль, как к ним будут пристраиваться комплементарные нуклеотиды или триплеты?
С этой трудностью уже умеют справляться некоторые большие рибозимы-полимеразы, выведенные ранее. Справился с ней и крошка QT45. Сначала ему давали произвольные матрицы с двуспиральными участками длиной в 4, 6 и 8 пар нуклеотидов. QT45 успешно реплицировал их, причем выход готового продукта (полных реплик предложенной матрицы) повышался при высоких концентрациях субстратов (триплетов). Дело в том, что для молекул РНК, способных скручиваться в трехмерные структуры с двойными спиралями, обычно характерно некоторое равновесие между скрученным и расправленным состояниями. Иначе говоря, они не всегда остаются скрученными, а иногда немножко раскручиваются. Вот тут-то и вступают в игру триплеты: они комплементарно пристраиваются к подходящим участкам раскрутившейся матрицы и мешают ей скрутиться обратно. Это помогает рибозиму-трипликазе делать свою работу.
Следующим подвигом QT45 стал синтез рабочей копии маленького, 33-нуклеотидного рибозима-эндонуклеазы Hammerhead. Репликация Hammerhead уже стала классикой в подобных исследованиях. Большой рибозим, способный реплицировать Hammerhead, впервые был выведен в 2011 году (см. Рибозимы могут размножать друг друга, «Элементы», 13.04.2011). Ну а сегодня полимеразу, не способную реплицировать Hammerhead, просто не будут воспринимать всерьез. Дошло до того, что некоторые большие рибозимы-полимеразы научились реплицировать Hammerhead с точностью, достаточной для полноценной эволюции без помощи белковых ферментов (см. Эволюция рибозимов, размножаемых рибозимами: еще один шаг к воссозданию РНК-жизни в пробирке, «Элементы», 27.03.2024).
Но большие рибозимы-полимеразы — гиганты по сравнению с Hammerhead. Этого нельзя сказать о QT45, который по размеру и структурной сложности лишь едва превосходит Hammerhead. И всё же QT45 справился с задачей. Правда, трудился он долго: целых 65 дней молчаливой работы в толще льда понадобилось ему, чтобы полностью (то есть на полную длину) отреплицировать матрицы Hammerhead с выходом конечного продукта 1,88%. Это значит, что 1,88% предоставленных ему праймеров были успешного достроены до полноразмерного Hammerhead. Да и это только в случае, когда в качестве субстратов ему дали лишь те 11 триплетов, которые необходимы для данной конкретной задачи. При наличии всех 64 триплетов выход конечного продукта снизился до 0,39%. Зато точность репликации оказалась на высоте: 92,6%. Это даже лучше, чем у многих больших полимераз. Для 33-нуклеотидного рибозима такая точность соответствует среднему числу ошибок 2,44 на одну копию Hammerhead. При этом 8,7% (1/e2,44) копий получаются идеальными — без единой ошибки.
Высокая точность объясняется эффектом «торможения на ошибке»: после присоединения не совсем комплементарного триплета дальнейшая репликация тормозится. В результате средняя точность репликации повышается ценой снижения выхода итогового продукта.
7. Триумф QT45: саморепликация
Размножение самого себя — весьма специфическая задача для рибозима-полимеразы. В некоторых отношениях она более сложна, чем репликация любой другой молекулы РНК той же длины. Отчасти поэтому ни одному рибозиму-полимеразе до сих пор не удавалось справиться с этой задачей. Хотя главная причина, конечно, в огромном размере этих рибозимов. Крохотный размер QT45 дал ему шанс стать первым рибозимом, осуществившим полный цикл саморепликации. И он этот шанс не упустил.
Саморепликация состоит из двух этапов. Сначала рибозим должен синтезировать свою комплементарную реплику (минус-цепь), используя себя в качестве матрицы. Затем он должен на матрице минус-цепи синтезировать копию себя (плюс-цепь).
Синтез минус-цепи ставит перед рибозимом два противоположных требования. С одной стороны, он должен быть скручен в устойчивую трехмерную конфигурацию, чтобы хорошо справляться с функцией рибозима. С другой стороны, он должен быть раскручен, чтобы хорошо справляться с функцией матрицы.
К счастью, молекул рибозима в каждой микрополости эвтектического льда много, и в каждый момент времени одни молекулы находятся в свернутом состоянии, а другие в развернутом. Баланс свернутости-развернутости зависит от концентрации триплетов, потому что триплеты комплементарно пристраиваются к подходящим участкам рибозима и мешают ему сворачиваться. Слишком высокие концентрации триплетов подавляют работу QT45, потому что он не может правильно свернуться, слишком низкие — тоже замедляют ее, потому что рибозиму не хватает субстратов для синтеза минус-цепи. Методом проб и ошибок исследователи подобрали оптимальную концентрацию триплетов и добились того, что рибозим за 72 дня синтезировал полноразмерные минус-цепи с выходом конечного продукта 0,24%. Из полученных минус-цепей 10,9% не содержали ни одной мутации, то есть репликация была довольно точной.
Полдела было сделано.
У второго этапа саморепликации — синтеза плюс-цепи на матрице минус-цепи — есть свой подводный камень. Он заключается в том, что рибозим (плюс-цепь) и матрица (минус-цепь) норовят сплестись в двойную спираль, которая является очень выгодным термодинамически и поэтому устойчивым, но бесполезным тупиковым продуктом.
Игры с концентрациями триплетов не помогли решить эту проблему. Оказалось, что плюс-цепь уверенно побеждает триплеты в конкуренции за право сплестись с минус-цепью. Тогда ученые решили, что нужно добавить в систему, помимо триплетов, такой субстрат, который будет сплетаться с минус-цепью с большим энтузиазмом, чем это делают триплеты. Они попробовали использовать гексамеры — маленькие РНК из шести нуклеотидов, то есть, по сути, два заранее сшитых триплета. Это сработало. Оказалось, что достаточно добавить в исходную смесь один-единственный активированный гексамер (pppAUUGAU, где ppp — три фосфата на 5’-конце), чтобы получить желаемый продукт — полноразмерные плюс-цепи1. Выход готового продукта за 72 дня — 0,17%, доля идеальных плюс-цепей без единой мутации 43,4%.
Таким образом, исследователи показали, что QT45 способен худо-бедно осуществлять оба этапа саморепликации. Он стал первым рибозимом, которому это удалось, а первопроходцам всегда трудно. Поэтому не нужно судить его слишком строго за медлительность и неточность, а лучше поздравить с великим достижением.
8. Что дальше?
Речь пока не идет о повторяющихся полноценных циклах саморепликации. Иными словами, ученые еще не могут завести у себя в лаборатории популяцию рибозимов, которая будет без постоянного вмешательства человека жить, размножаться и при этом не вырождаться под грузом мутаций. Однако путь к достижению этой амбициозной цели уже намечен. Основных проблем две.
Во-первых, чтобы процесс мог продолжаться, нужно своевременно расплетать двойные спирали, получающиеся в результате синтеза плюс-цепи на матрице минус-цепи и наоборот. Для этого нужны циклические изменения температуры и pH: в теплой слабокислой среде расплетаются цепи, в слабощелочном льду идет репликация. Можно представить себе такие циклы в какой-нибудь доисторической геотермальной системе, и, конечно, можно смоделировать их в лаборатории. Группа Холлигера уже научилась это делать, что позволило добиться экспоненциального размножения коротких РНК, реплицируемых большим рибозимом-полимеразой ().
Во-вторых, QT45 всё-таки недостаточно точен, чтобы избежать вырождения (мутационного коллапса) уже в первых нескольких циклах саморепликации. Но не будем забывать, что он совсем недавно родился «из ничего», из хаоса случайных последовательностей, от которого его отделяют лишь 18 раундов отбора. Так что с большой вероятностью потенциал рибозима QT45 еще не исчерпан, и его можно существенно улучшить. Пожелаем ему удачи.


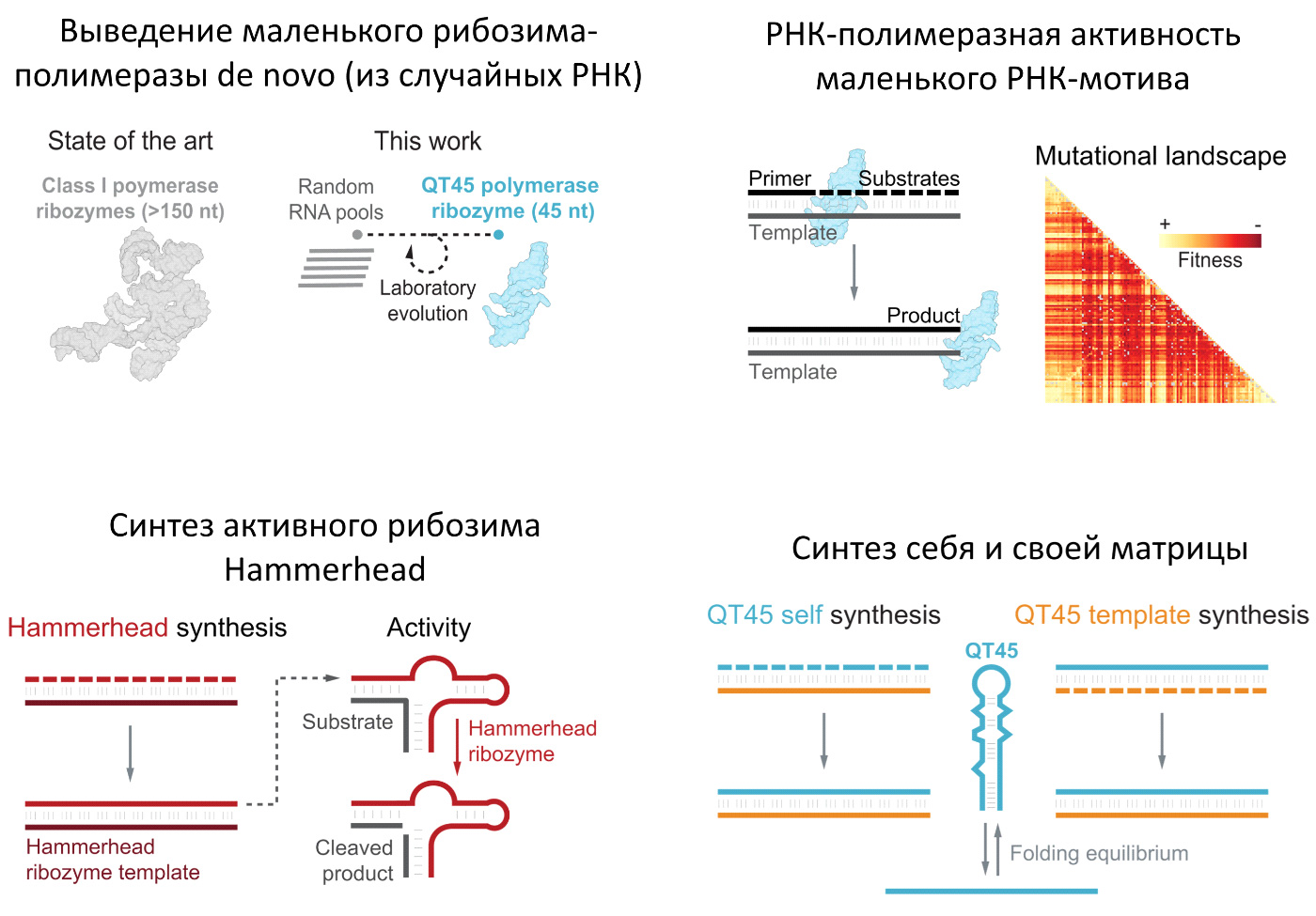
Рис. 1. Графическое резюме обсуждаемой статьи: маленький рибозим-полимераза QT45 и его достижения. Пояснения в тесте